Auch Aminocarbonsäuren genannt, sind Aminosäuren eine Gruppe organischer Verbindungen, deren strukturelle Aufbau aus Kohlenstoff-, Stickstoff-, Wasserstoff- und Sauerstoffatomen und einer variablen Seitenkettengruppe besteht. Sie sind bifunktionelle Verbindungen und ihre Moleküle enthalten Carboxylgruppen COOH und Aminogruppen NH2.

Die allgemeine Formel für Aminosäuren lautet:
NH2 – R – COOH
Der Name ist eine Abkürzung für den vollständigen Begriff α-Aminocarbonsäure. Wenn man über die verschiedenen Arten von Aminosäuren spricht, ist es üblich, die gebräuchlichen Namen der Verbindungen anstelle der systematischen Namen zu verwenden. Aminoessigsäure ist zum Beispiel Glycin, 2-Aminopropansäure ist Alanin und 2-Amino-3-methylbutansäure ist Valin.
Aufteilung der Aminosäuren
Die Hauptunterteilung der Aminosäuren ist die in proteinogene und nicht proteinogene Aminosäuren. Die erste Gruppe besteht aus etwa 20 Verbindungen, die alle ein Bestandteil von Proteinen sind und für den menschlichen Körper eine entscheidende Rolle spielen. Diese Proteine, die auch als Bausteine in Pflanzen und Tieren vorkommen, spielen eine grundlegende Rolle, da sie an vielen Mechanismen beteiligt sind, die für die Aufrechterhaltung der Homöostase im menschlichen Organismus verantwortlich sind. Eine andere Art der Kategorisierung berücksichtigt die Fähigkeit, die jeweilige Aminosäure zu produzieren oder die Notwendigkeit, sie dem menschlichen Körper mit der Nahrung zuzuführen.
Exogene und endogene Aminosäuren
Exogene Aminosäuren sind organische Verbindungen, die notwendig sind, um die Homöostase im Körper aufrechtzuerhalten, aber sie sind nicht in der Lage, sich selbst herzustellen. Daher ist es notwendig, sie in Form einer geeigneten Ernährung zusammen mit ausgewogenen Mahlzeiten und in Form von entsprechenden Nahrungsergänzungsmitteln zuzuführen. Zu dieser Gruppe von Aminosäuren gehören:
- Lysin, eine antivirale und immunstärkende Aminosäure;
- Methionin, das die Produktion von Wachstumshormonen reguliert;
- Threonin, das für die Aufrechterhaltung der Hautfeuchtigkeit und das reibungslose Funktionieren des Nervensystems verantwortlich ist;
- Leucin, dessen Hauptfunktion darin besteht, die Sekretion von Cortisol zu regulieren, den Zuckerspiegel zu regulieren und die Wundheilung zu fördern;
- Isoleucin, eine Aminosäure, die an den metabolischen Mechanismen der Muskeln beteiligt ist, wobei der Schwerpunkt auf den Muskelgeweben liegt;
- Valin, das die Muskelregeneration unterstützt und beim Abbau von überschüssigem Fettgewebe hilft;
- Tryptophan, eine Vorstufe von Serotonin, das die Schlafqualität und die Stimmung verbessert und den Appetit reguliert;
- Phenylalanin, das eine Vorstufe für eine Reihe wichtiger Hormone im Organismus ist, darunter Tyrosin, Dopamin, Epinephrin und Noradrenalin.
Die zweite Kategorie von Aminosäuren sind die endogenen Aminosäuren, deren Synthese im menschlichen Organismus regelmäßig stattfindet, so dass der Bedarf an ihnen ständig autark gedeckt ist. Diese Gruppe umfasst eine größere Anzahl von Aminosäuren, darunter:
- Alanin, eine Aminosäure, die für den Transport von Glukose zu den roten Blutkörperchen und dem Gehirn verantwortlich ist;
- Asparginsäure, die die geistige Leistungsfähigkeit verbessert und die Konzentrationsfähigkeit steigert;
- Asparagin, das zahlreiche Prozesse unterstützt, wie z.B. das Lernen, die Merkfähigkeit und die Verbesserung der Konzentration;
- Glutaminsäure, die den Verdauungsprozess unterstützt, die Müdigkeit verringert und das Gedächtnis stärkt.
Bedingt essentielle Aminosäuren
Dies sind Verbindungen, deren Herstellung im Organismus möglich ist, aber nur, wenn ihre Vorstufen in ausreichender Menge vorhanden sind. Dazu gehören:
- Arginin, das die Alterungsprozesse verlangsamt, die Geschwindigkeit der Wundheilung beeinflusst und die körperliche Leistungsfähigkeit verbessert;
- Cystein, das ein Baustein bei der Bildung von Glutathion und ein wichtiges Element bei der Herstellung von Kollagen ist;
- Glutamin, das die Darmfunktion unterstützt und den Organismus von unnötigen Stoffwechselprodukten reinigt;
- Tyrosin, das ebenso wie Cystein an der Kollagenproduktion beteiligt ist; es ist auch für die Melaninsynthese und für die Aufrechterhaltung der Schilddrüsenhomöostase unerlässlich;
- Glycin, eine Aminosäure mit therapeutischem Potenzial bei Arthritis und Diabetes;
- Ornithin, das die Fähigkeit hat, den Cortisolspiegel zu senken, die Schlafqualität zu verbessern und die Leistung des Darms und der Verdauungsenzyme zu steigern;
- Prolin, das den guten Zustand der Haut beeinflusst und ihre Elastizität verbessert;
- Serin, gerichtet auf Prozesse, die das Immunsystem und die Arbeit von Neuronen unterstützen.
Proteinogene Aminosäuren
Wie der Name schon sagt, gibt es auch Aminosäuren, die Bestandteile von Proteinen sind. Genauer gesagt handelt es sich bei Proteinen um Aminosäuren verschiedener Art, die miteinander verbunden sind. Es gibt zwanzig von ihnen, und während der Synthese werden sie durch so genannte Codons kodiert (Sequenzen von drei Nukleotiden, die in der mRNa enthalten sind und die kodierende Einheit bilden). Sie haben zwei Dinge gemeinsam: sie sind Alpha- und L-Aminosäuren. Das bedeutet, dass ihre Aminogruppe an das Alphakohlenstoffatom gebunden ist, das unmittelbar an die Carbonylgruppe angrenzt. Der Buchstabe „L“ hingegen bezeichnet das Stereoisomer in der Fisher-Projektion, so dass die Aminogruppe auf der linken Seite der Formel steht.
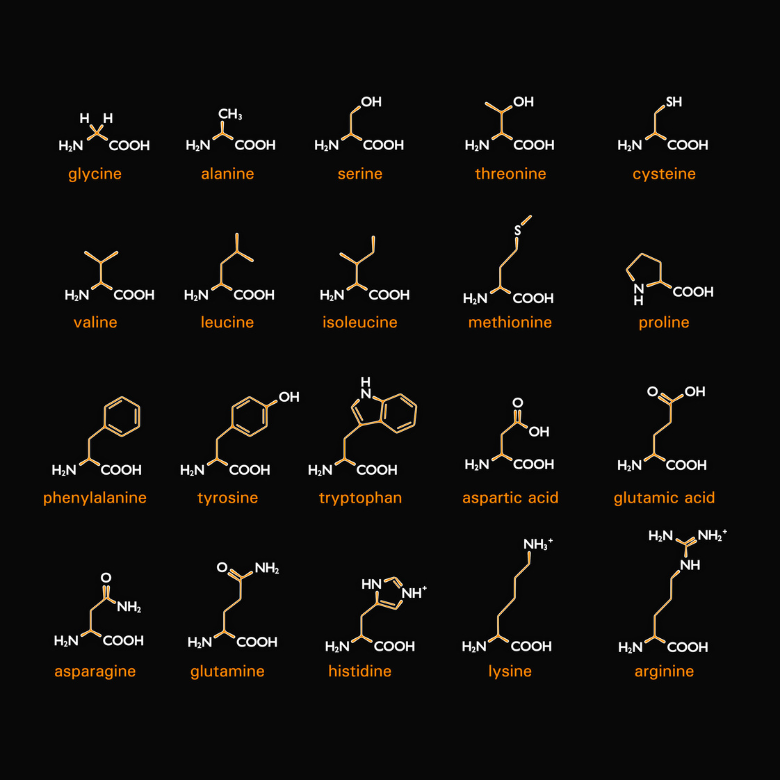
Physikalisch-chemische Eigenschaften von Aminosäuren
Die physische Form der Aminosäuren ist meist ein kristalliner Feststoff mit einem süßen Geschmack. Ihre Löslichkeit in Wasser ist gut, in organischen Lösungsmitteln sind sie jedoch unlöslich. Ihre Schmelzpunkte sind relativ hoch. Der chemische Charakter von Aminosäuren ist amphoter und die Reaktion von wässrigen Lösungen ist neutral. Sie dissoziieren zu hermaphroditischen Ionen, die durch Neutralisierung der basischen Aminogruppe mit Carboxylrest entstehen. Dies führt zur Bildung eines inneren Ammoniumsalzes, das beide Ladungen – positiv und negativ – aufweist. Ihre Menge ist gleich. Je nach der Umgebung, in der die Aminosäure dissoziiert, kann sie als Kation oder als Anion auftreten. Bei einer sauren Reaktion dissoziiert die Carboxylgruppe nicht, und die Aminosäure erhält eine positive Ladung. In einem alkalischen Medium verschiebt sich die Reaktion jedoch in Richtung der Bildung eines negativ geladenen Ions.
Isoelektrischer Punkt (pI)
Dies ist der Punkt, an dem die Aminosäure die Form eines hermaphroditischen Ions annimmt. Für jedes Molekül kann eine entsprechende Ionenkonzentration [H3O+] eingestellt werden, d.h. solch ein pH-Wert, bei dem keine Ionenwanderung im elektrischen Feld stattfindet. Die Amphoterie der Aminosäuren und ihr Vorkommen in Form eines hermaphroditischen Ions führen zu einer ionischen Struktur des Salzes, wenn es Säuren und Laugen ausgesetzt wird. Die experimentelle Bestimmung des isoelektrischen Punkts erfolgt durch Zugabe einer Aminosäure, z.B. Kasein, in entsprechende Reagenzgläser mit Lösungen (CH3COOH und CH3COONa) mit bekannten Konzentrationen von pH. Das Erreichen des isoelektrischen Punktes wird dort beobachtet, wo der am häufigsten vorkommende Niederschlag vorkommt. Aufgrund der Eigenschaften des isoelektrischen Punkts kann er zur Trennung eines Proteingemischs durch Elektrophorese verwendet werden. Die Methode beruht auf den Säure-Basen-Eigenschaften der Aminosäuren, und das Gemisch wird auf angefeuchtetes Papier gegeben. Bei der Verwendung eines bekannten pH-Werts können wir bestimmen, in welcher Form bestimmte Aminosäuren vorkommen werden. Wird dann eine Spannung an das Papier angelegt, wandern die positiv geladenen Aminosäuren zur Kathode (-) und die negativ geladenen zur Anode (+). Verbindungen mit einer neutralen Ladung, die durch die positiven und negativen Ladungen im Molekül ausgeglichen wird, bleiben an der gleichen Stelle.
Reaktionen, die für die Carboxylgruppe charakteristisch sind
- Veresterung, die in der Synthese von Estern besteht, die durch die Reaktion einer Aminosäure mit einem Alkohol entstehen. Das Reaktionsprodukt ist nicht amphoterer Natur, sondern weist die Eigenschaften des verwendeten Amins auf.
- Decarboxylierung, d.h. Erhitzen einer Aminosäure in Gegenwart einer Barium(II)-hydroxid (Ba(OH)2)-Lösung. Als Ergebnis dieser Umwandlung entstehen Amine.
- Komplexbildung, beruht auf der Fähigkeit von Aminosäuren, sich mit Metallkationen, hauptsächlich Kupfer, zu verbinden, wobei farbige Verbindungen – Komplexsalze – entstehen.

Reaktionen, die für die Aminogruppe charakteristisch sind
- Desaminierung, der Aminosäuren unterliegen, die in ihrer Struktur eine primäre Aminogruppe enthalten. Die Reaktion findet unter dem Einfluss von Salpetersäure (III) – HNO2 – statt, und die als Reaktant verwendete Aminosäure wird zu einer Hydroxysäure oxidiert. Die Aminogruppe wird als Stickstoff freigesetzt. Es gibt verschiedene Arten der Desaminierung, darunter hydrolytische, hydrolytische mit Decarboxylierung, Desaminierung durch Reduktion und desaturative Desaminierung.
- Oxidation, bei der Aminosäuren in Ketosäuren umgewandelt werden.
- Biochemische Reaktionen – alle Aminosäuren, die als Schiffsche Basen eingestuft werden können, weisen das Potenzial für biochemische Umwandlungen wie Transmittanz und Decarboxylierung auf.
Reaktionen zum Nachweis von Aminosäuren
- Die Ninhydrinreaktion ist eine Farbreaktion, bei der die Reaktanten eine Aminosäure und ein Reagenz in Form einer Ninhydrinlösung sind. Die Reaktion führt zu einer charakteristischen violett-blauen Färbung.
- Die Xanthoproteinreaktion ist ein Beispiel für einen Weg zum Nachweisen von aromatischen Aminosäuren, wie z.B. Phenylalanin, Tyrosin oder Tryptophan. Infolge der Einwirkung einer konzentrierten Lösung von Salpetersäure (V) – HNO3 auf die Verbindung wird eine gelbe Färbung beobachtet. Dies ist auf die Bildung von Nitroderivaten der Aminosäuren während der Reaktion zurückzuführen.
Quellen von Aminosäuren
Aufgrund des guten psychischen und physischen Gesundheitszustandes des menschlichen Organismus müssen die einzelnen Bausteine, einschließlich der Aminosäuren, in ausreichender Menge zur Verfügung stehen. Eine sehr wichtige Quelle aller Aminosäuren, die für das reibungslose Funktionieren notwendig sind, sind vollwertige Proteine. Dazu gehören Fleisch, insbesondere Geflügel und Fisch, Eier und Milchprodukte. In der Milch finden wir große Mengen an Leucin, Isoleucin, Threonin und Tryptophan. Lysin und Methionin finden wir in Sojabohnen. Valin liefern wir dem Körper mit Reis, Erdnüssen, Sesam und Mandeln, und Phenylalanin – indem wir Eier, Käse und Getreideprodukte in die Ernährung einführen. Das Vorkommen von Aminosäuren in Lebensmitteln ist weit verbreitet, aber für eine ausgewogene Ernährung sollten unterschiedliche Produkte verwendet werden. Das liegt daran, dass sie nur einige der Aminosäuren aus der Gruppe enthalten, die für die Aufrechterhaltung der richtigen Vitalfunktionen notwendig sind.