Definitionsgemäß ist Lumineszenz die Lichtemission von kalten Körpern, im Gegensatz zu Glühen, bei dem es sich um die Lichtemission von heißen Körpern handelt. Am einfachsten ausgedrückt, ist es Strahlung nicht-thermischen Ursprungs. Auf molekularer Ebene ist es ein Phänomen, das sich aus dem Übergang von Molekülen aus dem angeregten Zustand in den Grundzustand ergibt. Dieser Übergang führt zur Emission von Strahlung.
Jede vom System aufgenommene Energie muss wieder abgestrahlt werden. Dies kann auf verschiedene Weise geschehen, z.B. durch Lumineszenz, Wärme oder Konformationsänderungen in Molekülen. Laut dem Wissenschaftler Sergei Vavilov: „Lumineszenz ist der Überschuss der Strahlung eines Körpers über die Temperaturstrahlung desselben Körpers in einem bestimmten Spektralbereich und bei einer bestimmten Temperatur, die außerdem durch eine endliche Lumineszenzzeit gekennzeichnet ist, d.h. sie verschwindet nicht sofort nach Unterbrechung der Anregung.“
Arten der Lumineszenz
Man unterscheidet verschiedene Arten von Lumineszenz, die nach dem Faktor unterteilt werden, der sie zum Leuchten anregt. Die häufigsten sind:
- Photolumineszenz, wo das Anregungsmedium elektromagnetische Strahlung aus dem sichtbaren, ultravioletten oder infraroten Bereich ist. Die emittierte Energie in Form von Licht ist in der Regel geringer als die Anregungsenergie.
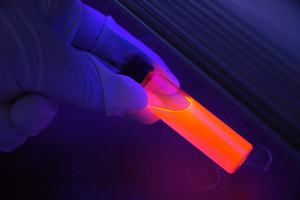
- Chemilumineszenz, bei der eine Substanz durch chemische Reaktionen angeregt wird, z.B. durch die Oxidation von Luminol, die dieses Phänomen verursacht. Es wird beim Nachweis von Blut an einem Tatort verwendet – es wird eine Mischung aus Luminol und Wasserstoffperoxid, einem starken Oxidationsmittel, versprüht.
- Die Biolumineszenz, die durch die Anregung von Stoffen infolge biochemischer Reaktionen gekennzeichnet ist, kann am Beispiel der Glühwürmchen beobachtet werden. In der Praxis wird diese Art der Strahlungsemission durch eine enzymatische Reaktion verursacht, die zur Oxidation von Luciferin durch Luciferase führt. Alle lebenden Organismen verfügen über die Fähigkeit zur Biolumineszenz, die jedoch meist zu gering ist, um wahrgenommen zu werden.
- Elektrolumineszenz, bei der die Anregung eines festen Moleküls in einem wechselnden oder konstanten elektrischen Feld erfolgt, während sie bei Gasen durch elektrische Entladung erfolgt. Dieses Phänomen wird unter anderem in Leuchtstofflampen, Elektrolumineszenzkondensatoren und Bildwandlern genutzt.
- Röntgenlumineszenz ist die Emission von Licht, das durch Röntgenstrahlen verursacht wird. Die zur Verbesserung der Bildqualität eingesetzten Verstärkungsbildschirme beruhen auf diesem Phänomen und verwenden Kalziumwolframat.
Darüber hinaus gibt es viele andere Arten von Lumineszenz, wie Radiolumineszenz, Elektronolumineszenz, Sonolumineszenz, Tribolumineszenz und Thermolumineszenz.
Photolumineszenz
Das in der chemischen Analyse am häufigsten verwendete Phänomen ist die Photolumineszenz. Man kann sie in zwei Hauptkategorien unterteilen, die sich nach den Mechanismen der Elektronenübergänge oder, bildlicher gesprochen, nach der Zeit zwischen Absorption und Emission von Energie unterscheiden. Diese sind:
- Fluoreszenz, ein kurzzeitiges Leuchten, bei dem von der Energieaufnahme bis zur Emission nicht mehr als 10-8s vergehen. Sie entsteht, wenn ein Elektron spontan von einem höheren Energieniveau in ein niedrigeres übergeht.
- Die Phosphoreszenz hingegen ist ein anhaltendes Leuchtphänomen, das mehr als 10-8s nach der Energieabsorption auftritt. Manchmal dauert es sogar mehrere Stunden oder Tage, bis sie Licht ausstrahlt. Diese Art von Energie erfordert das Vorhandensein von metatransmissiven Ebenen und wird mithilfe der thermischen Energie des Mediums erzeugt.
Die Fluoreszenz- und Phosphoreszenzenergien sind viel niedriger als die Energie der Anregungsstrahlung. Dies ist darauf zurückzuführen, dass die Energie des Moleküls durch nicht strahlende, thermische Übergänge abgebaut wird. Da die emittierten Photonen eine geringere Energie haben als die Anregungsphotonen, verschiebt sich das Emissionsspektrum in Richtung längerer Wellenlängen. Am stärksten verschoben ist das Spektrum der Phosphoreszenz, weil der Zustandsübergang des Moleküls nicht wie bei der Fluoreszenz vom Nullniveau des angeregten Singulett-Zustands S1, sondern vom Nullniveau des Triplett-Zustands T1 zu einem beliebigen Oszillations-Rotations-Niveau des Singulett-Grundzustands S0 erfolgt. Solche Übergänge können im Jabłonski-Diagramm grafisch dargestellt werden.

Fluoreszenz
Sie ist das am häufigsten verwendete Lumineszenzphänomen in der chemischen Analyse. Eine solche Strahlungsemission wird durch mehrere grundlegende Merkmale beschrieben, nämlich: das Absorptionsspektrum, das Fluoreszenzspektrum, die absolute Quantenausbeute der Fluoreszenz und die Emissionsdauer. Die absolute Quantenausbeute gibt das Verhältnis zwischen der Anzahl der emittierten Strahlungsquanten und der Anzahl der Quanten der Anregungsstrahlung an. Die Emissionsdauer hingegen ist die Zeit, die vergeht, bis die Fluoreszenzintensität auf einen bestimmten Wert abnimmt. Ein interessantes Phänomen ist auch die Konzentrationslöschung, die durch die Konzentrationsgrenze des Luminophors in der Lösung gekennzeichnet ist, jenseits derer die Fluoreszenz zu sinken beginnt. Luminophore sind chemische Verbindungen, die eine Lumineszenz aufweisen. Dazu gehören z.B. Polymere, Eosin, ZnS-Sulfide und Yttriumoxysulfide.
Photolumineszenz von organischen Verbindungen
Es stellt sich heraus, dass es eine Reihe von Regelmäßigkeiten gibt, die organische Moleküle in Bezug auf die Photolumineszenz aufweisen. Ihre Fluoreszenzbande ist gegenüber der Absorptionsbande in Richtung längerer Wellenlängen verschoben, aber die Spektren überschneiden sich teilweise. Es besteht auch eine proportionale Abhängigkeit zwischen Anregungslichtintensität, Absorptions- und Fluoreszenzquantenausbeute und Fluoreszenz. Dies ermöglicht den Einsatz in qualitativen und quantitativen Analysen. Die quantitative Analyse, die dieses Phänomen nutzt, wird als Spektrofluorimetrie bezeichnet. Die Technik hat eine niedrigere Nachweisgrenze als die Absorptionsspektrophotometrie und ist hoch selektiv. Die Selektivität ist darauf zurückzuführen, dass bestimmte chemische Verbindungen, Derivate von Arylverbindungen, die ein konjugiertes Doppelbindungssystem aufweisen, Fluoreszenz aufweisen. In der Praxis bedeutet dies, dass die Fluoreszenzeigenschaften der chemischen Verbindung umso stärker sind, je mehr aromatische Ringe in der Struktur enthalten sind. Zu den Anwendungen der Spektrofluorimetrie in der organischen Chemie gehören die Analyse von biologisch aktiven Verbindungen wie Vitaminen, Aminosäuren und Proteinen, von Arzneimitteln, einschließlich Antibiotika, von Lebensmitteln wie Kohlenhydraten und Fetten sowie von Umweltgiften wie PAK (polyzyklische aromatische Kohlenwasserstoffe).
Spektrofluorimetrie von anorganischen Verbindungen
Analysen innerhalb der anorganischen Chemie, die auf dem Phänomen der Fluorimetrie basieren, werden mit Hilfe eines Mechanismus zur Herstellung von Chelatkomplexen zwischen Elementen wie Aluminium, Beryllium, Magnesium, Kalzium und Seltenen Erden mit geeigneten organischen Liganden durchgeführt. Diese Komplexe weisen eine für sich spezifische Fluoreszenz auf und die Nachweisgrenzen der Methode sind sehr niedrig.
| Name des Reagens | Zu bestimmendes Element | Genauigkeit [μg·cm-1] |
| Salicylalo-o-aminophenol | Al
Ga Sb |
0,0005
0,15 0,2 |
| Lumonomagneson IREA | Mg | 0,002 |
| Morin | Fe
Th |
0,001
0,0004 |
Tabelle 1. Beispiele für Reagenzien, die für die fluorimetrische Bestimmung von Metallen verwendet werden, mit Angabe der Nachweisgrenze.