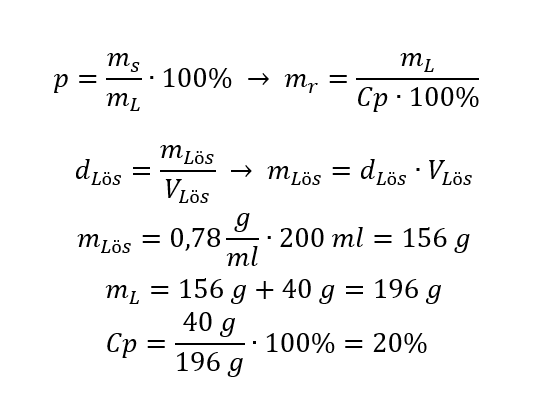In der Chemie werden häufig Begriffe wie "konzentrierte Lösung", "verdünnte Lösung" und "gesättigte Lösung" verwendet, die jedoch nur eine allgemeine Vorstellung davon vermitteln, ob eine Lösung viel oder wenig von einer Substanz enthält. Es gibt jedoch mehrere Methoden, um die Zusammensetzung einer Lösung quantitativ genau zu bestimmen. Eine davon wird im folgenden Artikel beschrieben.

Definition der prozentualen Konzentration
Der Begriff Konzentration bezieht sich auf die Menge einer Substanz in einer bestimmten Lösung. Die Konzentration kann in Einheiten angegeben werden, die von den verwendeten Mengen abhängen, wie Mol, Gramm oder Prozent. Die prozentuale Konzentration gibt an, wie viele Massenteile einer gelösten Substanz in 100 Massenteilen einer Lösung enthalten sind. Mit anderen Worten, es ist die Anzahl der Gramm der Substanz, die in 100 g der Lösung gelöst sind. Wenn wir zum Beispiel 3,2% Milch kaufen, bedeutet dies, dass in 100 g Milch 3,2 g Fett enthalten sind. Wir bezeichnen die prozentuale Konzentration mit dem Symbol Cp.
Allgemeine Formel für die prozentuale Konzentration
Um die Formel für die prozentuale Konzentration herzuleiten, ist es wichtig, sich daran zu erinnern, dass die Masse der Lösung (mL) nicht nur die Masse des Lösungsmittels (mLös), sondern auch die der darin gelösten Substanz (ms) ist:
mL = mLös + ms
Nimmt man eine 4%ige Lösung von 100 g als Beispiel, so weiß man, dass Cp = 4%, also die Masse der Substanz 4 g beträgt. Aus der Definition der prozentualen Konzentration ergibt sich, dass die Masse der Lösung 100 g beträgt und die Masse des Lösungsmittels 96 g.
Die prozentuale Konzentration kann mit der folgenden Formel berechnet werden:
Cp = (ms/mL) · 100%
Aus der Formel ergibt sich, dass man bei Kenntnis der Masse der Lösung und der Masse der Substanz leicht die prozentuale Konzentration berechnen kann. Wenn man zum Beispiel weiß, dass die Lösung eine Masse von 450 g hat und dass die darin gelöste Substanz 15 g beträgt, erhält man, wenn man dies in die Formel einsetzt:
Cp = (15/450) · 100% = 3,3%
Berechnung der Masse der einzelnen Bestandteile einer Lösung
Jede Formel, auch die für die prozentuale Konzentration, kann umgeformt werden. Kennt man die prozentuale Konzentration einer Lösung und ihre Masse, kann man die Masse der darin gelösten Substanz berechnen. Ebenso kann man mit der Kenntnis der prozentualen Konzentration und der Masse der Substanz die Masse der Lösung berechnen. Neben den Umformungen der Formeln ist es auch möglich, geeignete Proportionen zu verwenden.
Beispiel 1: Wie viele Gramm Zucker werden benötigt, um 300 g einer 10%igen Lösung herzustellen?
Aus dem Inhalt der Aufgabe wissen wir, dass die Masse der Lösung 300 g und ihre prozentuale Konzentration 10% beträgt. Um die Masse der gelösten Substanz zu bestimmen, gibt es zwei Möglichkeiten.
Methode 1 Umformung der Formel
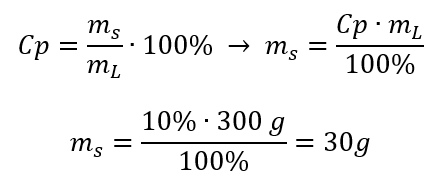
Methode 2 Verwendung der Proportionen in dem Wissen, dass eine 10%ige Lösung 10 g Zucker in 100 g Lösung enthält

Das Ergebnis beider Lösungsmethoden ist, dass für die Herstellung von 300 g der 10%igen Lösung 30 g Zucker verwendet werden müssen.

Beispiel 2. In wie viel Gramm Wasser müssen 10 g der Substanz aufgelöst werden, um eine 50%ige Lösung zu erhalten?
Aus dem Inhalt der Aufgabe wissen wir, dass die Masse der Substanz 10 g und die prozentuale Konzentration der Lösung 50 % beträgt. Das bedeutet, dass sich in 100 g Lösung 50 g der Substanz befinden. Die Bestimmung der Masse einer Lösung ist auf zwei Arten möglich. Beachten Sie, dass die Masse der Lösung nicht gleich der Masse des Lösungsmittels ist. Um die Masse des Lösungsmittels zu berechnen, subtrahiert man die Masse der Substanz von der Masse der Lösung.
Methode 1 Umformung der Formel
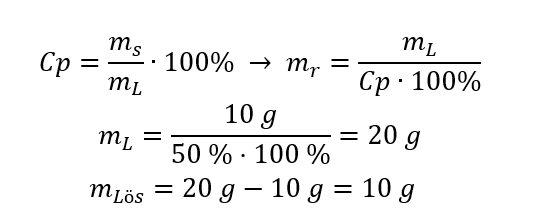
Methode 2 Verwendung der Proportionen in dem Wissen, dass sich in 100 g Lösung 50 g der Substanz befinden.
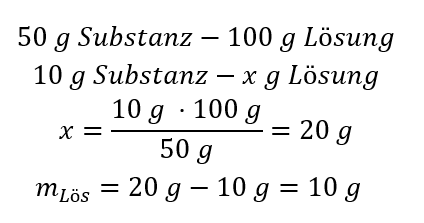
Die Lösung der Aufgabe mit den beiden Methoden lautet: Um eine 50%ige Lösung zu erhalten, müssen 10 g der Substanz in 10 g Wasser gelöst werden.
Zubereitung von Lösungen
Ein Schlüsselelement der Arbeit im Labor ist die Fähigkeit, Lösungen mit bestimmten Konzentrationen herzustellen. Dazu ist es notwendig, die Masse der Bestandteile zu kennen. Die zuvor berechnete Masse der Substanz muss in einem genau abgemessenen Volumen des Lösungsmittels gelöst werden. Das benötigte Volumen kann berechnet werden, wenn man die Masse und die Dichte der Flüssigkeit kennt. Die Dichte einer Lösung ist die charakteristische physikalische Größe einer Flüssigkeit, die ihre Masse für eine bestimmte Volumeneinheit bestimmt. Der Wert ist stark von der Temperatur abhängig. Wissend, dass die Dichte einer Lösung 2,03 g/ml beträgt, wissen wir, dass 1 ml der betreffenden Lösung eine Masse von 2,03 g hat. Die gebräuchlichsten Einheiten für die Dichte sind: g/ml = g/cm3, g/l = g/dm3, aber es gibt auch andere, z.B. kg/m3. Die Dichte einer Lösung wird durch die folgende Formel ausgedrückt: dL=mL/vL, wobei mL die Masse der Lösung und VL ihr Volumen ist. Wenn man das Volumen einer bestimmten Lösung und ihre Dichte kennt, kann man ihre Masse berechnen.
Beispiel 3. Welche Masse haben 20 ml einer Lösung, deren Dichte 1,201 g/ml beträgt?
Methode 1 Umformung der Formel
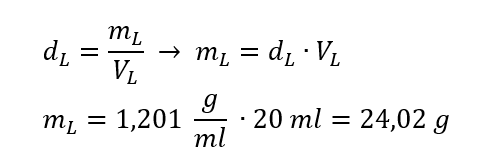
Methode 2 Verwendung der Proportionen in dem Wissen, dass 1,201 g der Lösung ein Volumen von 1 ml einnimmt
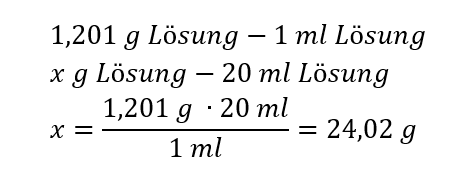
Beide Methoden zeigten, dass eine Lösung mit einer Dichte von 1,201 g/ml, die 20 ml einnimmt, eine Masse von 24,02 g hat.
Die Kenntnis des Begriffs der Dichte ermöglicht es uns, noch mehr Berechnungen zur prozentualen Konzentration durchzuführen.
Beispiel 4. Wie viel Gramm Salz sind in 10 ml einer 15%igen Lösung enthalten, wenn ihre Dichte 1,035 g/ml beträgt?
Methode 1 Umformung der Formel

Methode 2 Verwendung der Proportionen
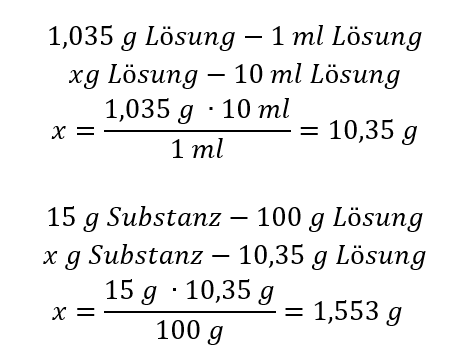
Beide Methoden ergaben, dass 1,553 g Salz abgewogen werden müssen, um 10 ml einer Lösung mit Cp = 15% und einer Dichte von 1,035 g/ml herzustellen.
Beispiel 5. Wie hoch ist die prozentuale Konzentration der Lösung, die man erhält, wenn man 40 g der Substanz in 200 ml Ethanol mit einer Dichte von 0,78 g/ml auflöst?
Um die Aufgabe zu berechnen, können wir die Umformung der Formel für die prozentuale Konzentration verwenden. Die Masse der Lösung kann berechnet werden, indem man die Masse der gelösten Substanz und die Masse des Lösungsmittels addiert. Da die Masse des Lösungsmittels in der Aufgabe nicht angegeben ist, wohl aber die Dichte und das Volumen, können wir die fehlenden Daten durch Umformung der Dichteformel berechnen.