Gli amminoacidi sono un gruppo di composti organici la cui struttura è costituita dagli atomi di carbonio, azoto, idrogeno e ossigeno, nonché da un gruppo a catena laterale variabile. Sono composti bifunzionali le cui molecole includono gruppi carbossilici COOH e gruppi amminici NH 2 .

La formula generale degli aminoacidi è la seguente: NH 2 – R – COOH Il loro nome è una forma abbreviata del termine “acido α-amminocarbossilico”. Quando parliamo di diversi tipi di aminoacidi, spesso sostituiamo i loro nomi sistematici con nomi consueti. Per fare un esempio, l’acido amminoacetico si chiama glicina, l’acido 2-amminopropanoico si chiama alanina e l’acido 2-ammino-3-metilbutanoico si chiama valina.
Classificazione degli aminoacidi
La divisione principale degli aminoacidi è in tipi proteici e non proteici. Il primo gruppo comprende circa 20 composti, ciascuno dei quali è un componente delle proteine ed è fondamentale per il corpo umano. Queste proteine, che esistono anche come molecole strutturali nelle piante e negli animali, svolgono un ruolo fondamentale prendendo parte a numerosi meccanismi responsabili del mantenimento dell’omeostasi nel corpo umano. Un’altra classificazione tiene conto della possibilità di produrre un particolare amminoacido o del suo apporto necessario al corpo umano insieme al cibo.
Amminoacidi esogeni ed endogeni
Gli amminoacidi esogeni sono composti organici necessari per mantenere l’omeostasi nel nostro corpo, ma non sono in grado di autoprodursi. Per questo motivo devono essere forniti sotto forma di un’alimentazione adeguata, accompagnata da pasti adeguatamente bilanciati e sotto forma di adeguati integratori. Questo gruppo di aminoacidi comprende:
- Lisina – un amminoacido anti-virus che migliora l’immunità;
- Metionina, che controlla la produzione dell’ormone della crescita;
- Treonina, responsabile del corretto mantenimento dell’umidità della pelle e del corretto funzionamento del sistema nervoso;
- Leucina, il cui ruolo principale è controllare il livello di cortisolo secreto e i livelli di zucchero, nonché favorire la guarigione delle ferite;
- Isoleucina – un aminoacido che partecipa ai processi del metabolismo muscolare, con particolare attenzione ai tessuti muscolari;
- Valina, che supporta il recupero muscolare e la rimozione del tessuto adiposo in eccesso;
- Triptofano, precursore della serotonina, che ha il compito di aumentare la qualità del sonno, migliorare lo stato fisico e mentale e controllare l’appetito;
- La fenilalanina, essendo un precursore di molti ormoni importanti per il corpo umano, tra cui tirosina, dopamina, epinefrina e noradrenalina.
L’altra categoria comprende gli aminoacidi endogeni , che vengono sintetizzati regolarmente nel corpo umano, quindi il loro fabbisogno è costantemente coperto in modo autonomo. Questo gruppo contiene più aminoacidi, che includono:
- Alanina – un amminoacido responsabile del trasporto del glucosio ai globuli rossi e al cervello;
- Acido aspartico, che migliora le funzioni cognitive e la capacità di concentrazione;
- Asparagina, che supporta molti processi come l’apprendimento, la memorizzazione o il miglioramento della concentrazione;
- L’acido glutammico, che supporta i processi di digestione, riduce la sensazione di stanchezza e sostiene la memoria.
Aminoacidi condizionali
Si tratta di composti che possono essere prodotti nell’organismo, ma solo in caso di accesso a quantità adeguate dei loro precursori. Gli amminoacidi condizionali includono:
- Arginina, che ritarda l’invecchiamento, riduce i tempi di guarigione delle ferite e migliora la forma fisica;
- Cisteina, che è un materiale da costruzione nella formazione del glutatione ed è un importante elemento di produzione del collagene;
- Glutammina, che supporta il funzionamento dell’intestino e la rimozione dei prodotti metabolici non necessari dal corpo umano;
- Tirosina, che, come la cisteina, partecipa alla produzione del collagene, ma è necessaria anche per la sintesi della melanina e aiuta a mantenere l’omeostasi della tiroide;
- Glicina, che è un amminoacido capace di curare l’artrite e il diabete;
- L’ornitina, che è in grado di ridurre il livello di cortisolo, migliorare la qualità del sonno e potenziare l’efficienza delle funzioni intestinali e degli enzimi digestivi;
- Prolina, che influisce favorevolmente sulla condizione della pelle e ne migliora la flessibilità;
- Serina, orientata ai processi che supportano il sistema immunitario e il funzionamento dei neuroni.
Aminoacidi proteici
Come suggerisce il nome, ci sono anche aminoacidi che sono componenti delle proteine. Più specificamente, le proteine sono vari tipi di amminoacidi combinati tra loro. Sono venti e durante la sintesi vengono codificati dai cosiddetti codoni (sequenze di tre nucleotidi contenute nell’mRNa, che costituiscono l’unità codificante). Ognuno di essi ha due caratteristiche comuni: sono alfa e L-amminoacidi. Ciò significa che il loro gruppo amminico è collegato al carbonio alfa, che confina direttamente con il gruppo carbonilico. La lettera "L" sta per uno stereoisomero nella proiezione di Fischer, quindi il gruppo amminico si trova sul lato sinistro della formula. 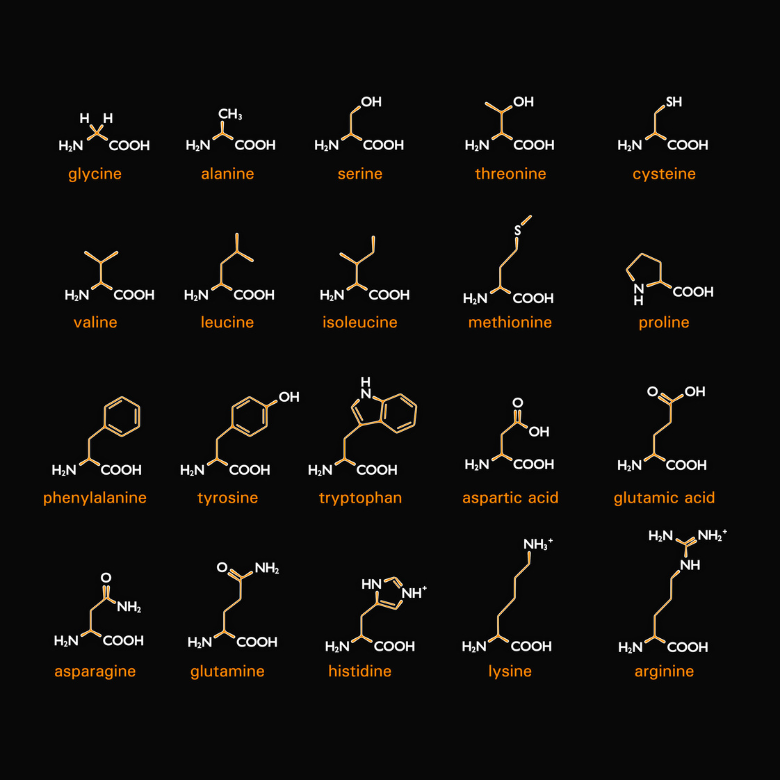
Le proprietà fisico-chimiche degli amminoacidi
La forma fisica degli amminoacidi è solitamente un solido cristallino dal sapore dolce. La loro solubilità in acqua è buona, ma non si dissolvono nei solventi organici. I loro punti di fusione sono relativamente alti. La natura chimica degli amminoacidi è anfotera e la reazione delle loro soluzioni acquose è neutra. La dissociazione produce ioni doppi, che sono il risultato della neutralizzazione del gruppo amminico basico con un radicale carbossilico. Ciò si traduce nella produzione di un sale di ammonio interno che mostra entrambe le cariche: positiva e negativa. Le loro quantità sono uguali. Un amminoacido può esistere come catione o anione, a seconda dell’ambiente in cui si dissocia. Per le reazioni acide, il gruppo carbossilico non si dissocia e l’amminoacido ha una carica positiva. In un ambiente alcalino, le reazioni si spostano verso la produzione di uno ione negativo.
Il punto isoelettrico (pI)
È un punto in cui un amminoacido assume la forma di un doppio ione. Per ogni molecola possiamo regolare una concentrazione adeguata di ioni [H 3 O +], ovvero un pH tale per cui gli ioni non si muovono nel campo elettrico. La natura anfotera degli amminoacidi e la loro esistenza sotto forma di ioni doppi implica una struttura ionica dei sali quando colpiti da acidi e alcali. La determinazione sperimentale del punto isoelettrico viene effettuata aggiungendo un amminoacido, ad esempio la caseina, in apposite provette contenenti soluzioni (CH 3 COOH e CH 3 COONa) a concentrazioni di pH note. Il punto isoelettrico viene raggiunto dove il deposito è più abbondante. Data la caratteristica del punto isoelettrico, possiamo utilizzarlo per separare una miscela di proteine con l’utilizzo dell’elettroforesi. Questo metodo si basa sulle proprietà acido-basiche degli aminoacidi e la miscela viene posta su carta bagnata. Utilizzando un pH noto, possiamo determinare la forma in cui esisteranno particolari amminoacidi. Quindi, se diamo tensione alla carta, gli amminoacidi con carica positiva si sposteranno verso il catodo (-), e quelli con carica negativa, verso l’anodo (+). I composti con carica neutra, bilanciati dalle cariche positive e negative nella molecola, rimarranno nello stesso posto.
Reazioni caratteristiche del gruppo carbossilico
- Esterificazione, che consiste nel sintetizzare esteri prodotti da una reazione tra un amminoacido e un alcol. Il prodotto di tale reazione non presenta natura anfotera, ma presenta le proprietà dell’ammina utilizzata.
- Decarbossilazione, cioè il riscaldamento di un amminoacido in presenza di una soluzione di idrossido di bario (II) (Ba(OH) 2 ). La trasformazione produce ammine.
- La produzione di complessi è legata alla capacità degli amminoacidi di legarsi ai cationi di un metallo, principalmente il rame, provocando la formazione di composti colorati (sali complessi).

Reazioni caratteristiche del gruppo amminico
- Deaminazione, che riguarda gli amminoacidi che contengono il gruppo amminico primario. La reazione avviene sotto l’influenza dell’acido nitrico (III) (HNO 2 ) e l’amminoacido utilizzato come reagente si ossida e produce un idraacido. Il gruppo amminico viene rilasciato sotto forma di azoto. Esistono diversi tipi di deaminazione, inclusa la deaminazione idrolitica, la deaminazione idrolitica con decarbossilazione, la deaminazione per riduzione e la deaminazione per desaturazione.
- Ossidazione, che provoca la conversione degli amminoacidi in chetoacidi.
- Reazioni biochimiche: tutti gli amminoacidi che possono essere classificati come basi di Schiff sono capaci di trasformazioni biochimiche come trasmittanza e decarbossilazione.
Reazioni utilizzate per rilevare gli amminoacidi
- La reazione della ninidrina è una reazione colorata in cui i reagenti sono un amminoacido e un reagente sotto forma di soluzione di ninidrina. La reazione produce un caratteristico colore viola-blu.
- La reazione della xantoproteina è un esempio del percorso per rilevare gli aminoacidi aromatici, come la fenilalanina, la tirosina o il triptofano. Un composto sottoposto ad una soluzione concentrata di acido nitrico (V) (HNO 3 ) cambia colore in giallo. È il risultato della produzione di derivati dell’amminoacido nitrico durante la reazione.
Fonti di aminoacidi
Per garantire una buona condizione fisica e mentale del corpo umano, dovremmo fornirgli quantità adeguate di ciascun materiale da costruzione, compresi gli aminoacidi. Una fonte estremamente importante di tutti gli aminoacidi necessari per il corretto funzionamento sono le proteine complete. Includono carne, in particolare pollame, pesce, uova e latticini. Il latte contiene elevate quantità di leucina, isoleucina, treonina e triptofano. La lisina e la metionina si trovano nella soia. La valina può essere fornita insieme a riso, arachidi, sesamo e mandorle, mentre la fenilalanina, inserendo nella nostra dieta uova, formaggi e prodotti a base di cereali. La presenza di aminoacidi nei prodotti alimentari è comune, ma affinché la nostra dieta sia adeguatamente bilanciata è necessario diversificare i prodotti che utilizziamo. Questo perché contengono solo alcuni aminoacidi del gruppo necessari per mantenere le corrette funzioni vitali.
