불화칼슘(형석)은 의심할 여지 없이 가장 잘 알려져 있고 가장 가치 있는 무기 화합물 중 하나입니다. 고유한 특성으로 인해 가정용 및 산업용 플랜트에서 다양한 용도로 사용됩니다. 불화 칼슘의 특징은 무엇이며 어디에 사용됩니까? 확인해 봅시다.

불화물이란 무엇입니까?
불화칼슘 또는 불화칼륨과 같은 화합물은 집합적으로 불화물이라고 하는 그룹에 속합니다. 그들은 불소를 포함하는 무기 불산 염입니다. 평균적인 소비자는 학교와 유치원에서 예방적으로 제공되는 불소화 치료와 불소만을 연관시킬 것입니다. 실제로, 이 화합물은 치약, 구강 세정제 및 치아 법랑질 강화 제제의 성분으로서 불소 함량으로 인해 가장 인기가 있습니다.
불화 칼슘 : 생산 및 특성
불화칼슘이란? 화합물의 분자식은 CaF 2 이고 체계적인 이름은 이불화칼슘입니다. 이 물질은 작고 반짝이며 유리질의 결정으로 나타나며 이성분의 불화수소산과 탄산칼슘 의 반응을 통해 얻습니다. CaF 2 는 형석이라고 하는 일반적인 광물로 자연적으로 발생합니다. 형석 결정은 분홍색에서 녹색 및 파란색에 이르기까지 다양한 색상을 가지고 있습니다. 그리고 형석 칼슘의 물리적 및 화학적 특성은 무엇입니까? 이 화합물은 물에 대한 용해도가 낮습니다. 그것은 산에 거의 녹지 않으며 열악한 전기 전도체입니다. 불화칼슘의 분자량은 78.08g/mol이고 밀도는 3.18g/cm³(20°C)입니다. CaF 2 결정체는 1418ºC의 온도에서 녹기 시작하여 2500ºC에서 끓습니다. 이 물질은 다른 물질의 부식을 일으키고 황산 (VI)과 반응합니다. 불화 칼슘은 칼슘 양이온과 불소 음이온으로 해리 됩니다.
불화칼슘의 응용
불화 칼슘은 산업 및 그 이상에서 널리 사용됩니다. 이 화합물은 주로 유리 에칭 및 효모 생산에 사용되는 불화수소 생산에 적합합니다. CaF 2 는 화학 실험실에서 시약 으로 유용합니다. 또한 다음 제품의 생산에 사용되는 귀중한 원료입니다.
- 필터 및 광학 안경,
- 반사 방지 코팅,
- 화장품,
- (칼슘) 농업에 사용되는 질소 비료,
- 치과 준비 및 바니시.
불소와 그 화합물인 불화칼슘과 불화나트륨은 충치 예방에 매우 다양한 용도로 사용됩니다. 그들은 치아 법랑질을 강화하고 산으로부터 보호하는 젤, 구강 세척제 및 페이스트를 생산하는 데 사용됩니다. 이 물질은 구강과 및 미용 의학에 사용됩니다. 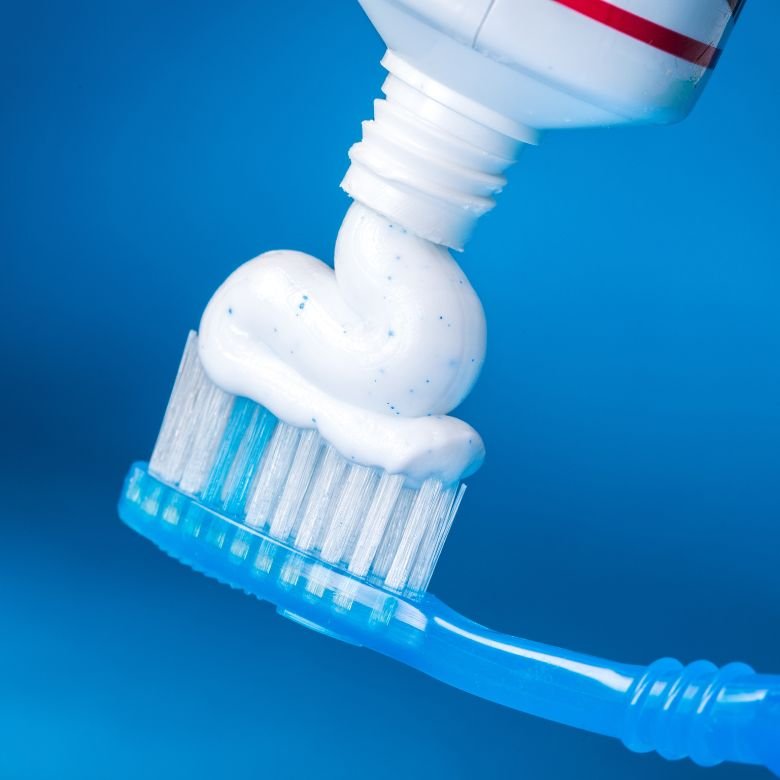
불화칼슘 – 유해성
불화칼슘은 해로운가요? 다른 화학 물질과 마찬가지로 불화칼슘도 잘못 사용하면 호흡기 및 소화기 계통에 여러 가지 불쾌한 질병을 유발할 수 있습니다. 실험실 조건에서 CaF 2 흄의 흡입은 내부 장기의 화상을 유발하고 심지어 폐부종을 유발합니다. 불화칼슘의 소화로 인한 위험은 무엇입니까? 크리스탈은 복통, 설사 및 사지의 따끔거림을 포함하는 증상이 있는 확산 중독을 일으킵니다. 불화칼슘과 눈 점막의 접촉은 발적과 작열감을 유발합니다. 그러나 소량의 CaF 2 는 제조업체에서 권장하는 대로 사용할 경우 부작용이 없습니다.
불화칼슘에 대한 몇 가지 정보
자연에서 발생하는 형석에는 여러 이름이 있습니다. 광부들은 그것을 spar 또는 river spar라고 부릅니다. 불화 칼슘은 신체의 모든 기관, 특히 근육과 뼈의 기능을 향상시키는 건강 보조 식품의 생산에 사용됩니다. CaF2 를 함유한 분말은 면역 체계를 자극하고 전신의 물-미네랄 균형의 질을 향상시키는 치료에 사용됩니다.
- https://chemicalsafety.ilo.org/dyn/icsc/showcard.display?p_lang=pl&p_card_id=1323&p_version=2
- https://pubchem.ncbi.nlm.nih.gov/compound/Calcium-Fluoride
- https://www.britannica.com/science/calcium-fluoride
