Por definição, luminescência é a emissão de luz por objetos frios, em oposição à incandescência, que é a emissão de luz por objetos quentes. Simplificando, é a radiação de origem não térmica. Em termos moleculares, é um fenômeno resultante da transição de moléculas de um estado excitado para o estado básico. Como resultado dessa transição, a radiação é emitida.
Qualquer energia absorvida pelo sistema deve ser emitida. Ocorre de várias maneiras, por exemplo, na forma de luminescência, calor ou mudanças conformacionais nas moléculas. Segundo o cientista Sergei Vavilov: "A luminescência é o excesso de radiação de um corpo sobre a radiação de temperatura do mesmo corpo em uma determinada região espectral e em uma determinada temperatura, que também é caracterizada por um tempo de iluminação finito, ou seja, não desaparece imediatamente após a interrupção da excitação."
Tipos de luminescência
Distinguimos diferentes tipos de luminescência de acordo com o fator que os excita a iluminar. Os mais populares são:
- Fotoluminescência, onde o fator de excitação é a radiação eletromagnética do espectro visível, ultravioleta ou infravermelho. A energia emitida, na forma de luz, costuma ser menor que a energia de excitação.
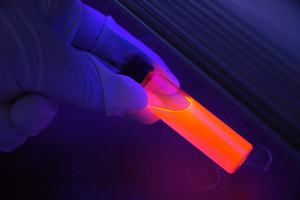
- A quimioluminescência, onde uma substância é excitada por reações químicas, esse fenômeno ocorre, por exemplo, devido à oxidação do luminol. É usado para a detecção de sangue na cena do crime – uma mistura de luminol eperóxido de hidrogênio – um forte oxidante – é pulverizado.
- A bioluminescência, caracterizada pela excitação de substâncias como resultado de reações bioquímicas, pode ser observada em vaga-lumes. Na prática, esse tipo de emissão de radiação é causado por uma reação enzimática que leva à oxidação da luciferina pela luciferase. Todos os organismos vivos têm o potencial de bioluminescência, mas geralmente é muito baixo para ser notado.
- Eletroluminescência, onde a excitação de um sólido ocorre em um campo elétrico alternado ou constante, enquanto os gases sofrem eletroluminescência sob descargas elétricas. Este fenômeno é utilizado, entre outros, em lâmpadas fluorescentes, capacitores eletroluminescentes e conversores de imagem.
- A luminescência de raios X é a emissão de luz causada pelos raios X. As telas de aprimoramento usadas para melhorar a qualidade da imagem são baseadas nesse fenômeno, usando tungstato de cálcio.
Além disso, existem muitos outros tipos de luminescência, como radioluminescência, luminescência estimulada por elétrons, sonoluminescência, triboluminescência e termoluminescência.
Fotoluminescência
A fotoluminescência é o fenômeno mais frequentemente usado em análises químicas. Pode ser categorizado em duas categorias principais de acordo com os mecanismos de transições eletrônicas, ou mais claramente de acordo com o tempo entre a absorção e a emissão de energia. Estes são:
- Fluorescência, que é uma iluminação de curto prazo, onde não passam mais de 10 -8 segundos desde a absorção de energia até a emissão. Ocorre no caso de uma transição espontânea de um nível de energia mais alto de um elétron para um mais baixo.
- A fosforescência é um fenômeno de iluminação de longa duração, que ocorre em um tempo superior a 10 -8 s a partir da absorção de energia. Às vezes, leva horas ou dias para emitir luz. Este tipo de energia requer a existência de níveis metaestáveis e é criada com a participação da energia térmica do meio.
A energia de fluorescência e fosforescência é muito menor do que a energia da radiação de excitação. Resulta da degradação energética da molécula através de transições térmicas não radiativas. Como os fótons emitidos têm energia menor que os de excitação, o espectro de emissão se desloca para comprimentos de onda mais longos. O espectro de fosforescência é o mais deslocado, porque a transição do estado molecular ocorre não do nível do estado singleto excitado zero S 1 como no caso da fluorescência, mas do nível do estado triplete zero T 1 para qualquer estado oscilatório- nível de rotação do estado fundamental singleto S 0 . Tais transições podem ser observadas graficamente no diagrama de Jablonski. 
Fluorescência
A fluorescência é o fenômeno de luminescência mais frequentemente usado em análises químicas. Tal emissão de radiação é descrita por várias características básicas, ou seja: espectro de absorção, espectro de fluorescência, eficiência quântica de fluorescência absoluta e duração da emissão. O rendimento quântico absoluto é a razão entre o número de quanta da radiação emitida e o número de quanta da radiação de excitação. A duração da emissão é o tempo em que a intensidade da fluorescência decai para um determinado valor. A têmpera por concentração também é um fenômeno interessante. É caracterizada pelo limite de concentração do fósforo na solução, além do qual a fluorescência começa a diminuir. Um fósforo é um composto químico que exibe luminescência. Estes são, por exemplo, polímeros, eosina, sulfetos de ZnS e oxissulfetos de ítrio.
Fotoluminescência de compostos orgânicos
Acontece que existem muitas regularidades que as moléculas orgânicas apresentam em relação à fotoluminescência. Sua banda de fluorescência é deslocada em relação à banda de absorção para comprimentos de onda mais longos, mas os espectros se sobrepõem parcialmente. Existe também uma relação proporcional entre a intensidade da luz de excitação, absorção e rendimento quântico de fluorescência e fluorescência. Portanto, é possível utilizá-lo em análises qualitativas e quantitativas. A análise quantitativa usando esse fenômeno é chamada de espectrofluorimetria. A técnica tem um limite de detecção mais baixo em comparação com a espectrofotometria de absorção e é altamente seletiva. A seletividade resulta do fato de que compostos químicos específicos, derivados de compostos arílicos, tendo um sistema conjugado de ligações duplas, sofrem fluorescência. Na prática, isso significa que quanto mais anéis aromáticos na estrutura, mais fortes são as propriedades fluorescentes do produto químico. A aplicação da espectrofluorimetria na química orgânica inclui a análise de compostos biologicamente ativos, como vitaminas, aminoácidos , proteínas; produtos farmacêuticos, incluindo antibióticos; compostos alimentares, como carboidratos e gorduras , e tóxicos ambientais, como PAHs (hidrocarbonetos aromáticos policíclicos).
Espectrofluorimetria de compostos inorgânicos
Ensaios de química inorgânica baseados no fenômeno da fluorimetria são realizados utilizando o mecanismo de formação de complexos quelatos entre elementos como alumínio, berílio, magnésio, cálcio e elementos de terras raras com ligantes orgânicos apropriados. Esses complexos exibem uma fluorescência específica e os limites de detecção são muito baixos.
| Reagente | elemento ensaiado | Sensibilidade [ μg·cm -1] |
| Salicil-o-aminofenol | Al Ga Sb | 0,0005 0,15 0,2 |
| IREA lumonomagnesona | mg | 0,002 |
| morin | Fe Th | 0,001 0,0004 |
Tabela 1. Exemplos de reagentes usados para a determinação fluorimétrica de metais e LoD.
