Amino asitler, yapısı karbon, nitrojen, hidrojen ve oksijen atomlarının yanı sıra değişken bir yan zincir grubundan oluşan bir grup organik bileşiktir. Molekülleri COOH karboksil grupları ve NH2 amin grupları içeren iki işlevli bileşiklerdir.

Amino asitlerin genel formülü şu şekildedir: NH 2 – R – COOH Adları “α-amino karboksilik asit” teriminin kısaltılmış halidir. Farklı amino asit türleri hakkında konuştuğumuzda, genellikle onların sistematik isimlerini geleneksel isimlerle değiştiririz. Örnek vermek gerekirse aminoasetik asit glisin, 2-aminopropanoik asit alanin ve 2-amino-3-metilbütanoik asit ise valin olarak adlandırılır.
Amino asitlerin sınıflandırılması
Amino asitlerin ana bölümü proteinli ve proteinsiz tiplere ayrılmıştır. İlk grup, her biri proteinlerin bir bileşeni olan ve insan vücudu için çok önemli olan yaklaşık 20 bileşiği içerir. Bitkilerde ve hayvanlarda da yapısal molekül olarak bulunan bu proteinler, insan vücudunda homeostazın korunmasından sorumlu birçok mekanizmada görev alarak temel rol oynarlar. Başka bir sınıflandırma, belirli bir amino asidin üretilme olasılığını veya gıdayla birlikte insan vücuduna gerekli tedariki dikkate alır.
Ekzojen ve endojen amino asitler
Ekzojen amino asitler vücudumuzda homeostazisin sağlanması için gerekli olan ancak kendi kendine üretim kabiliyeti olmayan organik bileşiklerdir. Bu nedenle bunların uygun bir diyetle, uygun şekilde dengelenmiş öğünlerle ve yeterli takviyelerle sağlanması gerekir. Bu amino asit grubu şunları içerir:
- Lizin – bağışıklığı artıran bir anti-virüs amino asidi;
- Büyüme hormonunun üretimini kontrol eden metiyonin;
- Cilt neminin uygun şekilde korunmasından ve sinir sisteminin düzgün işleyişinden sorumlu olan treonin;
- Başlıca görevi salgılanan kortizol ve şeker düzeyini kontrol etmek ve yara iyileşmesini desteklemek olan Lösin;
- İzolösin – özellikle kas dokularına odaklanarak kas metabolizması süreçlerinde yer alan bir amino asit;
- Kas toparlanmasını ve fazla yağ dokusunun uzaklaştırılmasını destekleyen valin;
- Uyku kalitesini artıran, fiziksel ve zihinsel durumu iyileştiren ve iştahı kontrol eden bir serotonin öncüsü olan triptofan;
- Fenilalanin, tirozin, dopamin, epinefrin ve noradrenalin dahil olmak üzere insan vücudu için önemli olan birçok hormonun öncüsüdür.
Diğer kategori, insan vücudunda düzenli olarak sentezlenen endojen amino asitleri içerir, dolayısıyla bunlara olan talep sürekli olarak özerk bir şekilde karşılanır. Bu grup aşağıdakileri içeren daha fazla amino asit içerir:
- Alanin – glikozun kırmızı kan hücrelerine ve beyne taşınmasından sorumlu bir amino asit;
- Bilişsel işlevleri ve konsantre olma yeteneğini geliştiren aspartik asit;
- Öğrenme, ezberleme, konsantrasyon geliştirme gibi birçok süreci destekleyen asparajin;
- Sindirim süreçlerini destekleyen glutamik asit, yorgunluk hissini azaltır ve hafızayı destekler.
Koşullu amino asitler
Bunlar vücutta üretilebilen ancak öncüllerinin uygun miktarda alınması durumunda üretilebilen bileşiklerdir. Koşullu amino asitler şunları içerir:
- Yaşlanmayı geciktiren, yaraların iyileşme süresini kısaltan ve fiziksel kondisyonu artıran arginin;
- Glutatyonun oluşumunda yapı malzemesi olan ve kolajenin önemli bir üretim elemanı olan sistein;
- Bağırsakların işleyişini ve gereksiz metabolik ürünlerin insan vücudundan atılmasını destekleyen Glutamin;
- Tıpkı sistein gibi kollajen üretiminde yer alan ancak aynı zamanda melanin sentezi için de gerekli olan ve tiroid bezinin homeostazisinin korunmasına yardımcı olan tirozin;
- Artrit ve diyabeti iyileştirebilen bir amino asit olan glisin;
- Kortizol seviyesini azaltabilen, uyku kalitesini artıran, bağırsak fonksiyonlarının ve sindirim enzimlerinin etkinliğini artıran ornitin;
- Cildin durumunu olumlu yönde etkileyen ve esnekliğini artıran prolin;
- Serin, bağışıklık sistemini ve nöronların işleyişini destekleyen süreçlere yöneliktir.
Protein amino asitleri
Adından da anlaşılacağı gibi proteinlerin bileşeni olan amino asitler de vardır. Daha spesifik olarak proteinler, birbirleriyle birleştirilmiş çeşitli amino asit türlerinden oluşur. Bunlardan yirmi tane vardır ve sentez sırasında kodonlar (kodlama birimini oluşturan mRNA’da bulunan üç nükleotid dizisi) tarafından kodlanırlar. Her birinin iki ortak özelliği vardır: bunlar alfa ve L-amino asitlerdir. Bu, amin gruplarının doğrudan karbonil grubuna bitişik olan alfa-karbona bağlı olduğu anlamına gelir. "L" harfi Fischer projeksiyonunda bir stereoizomeri temsil eder, dolayısıyla amin grubu formülün sol tarafında bulunur. 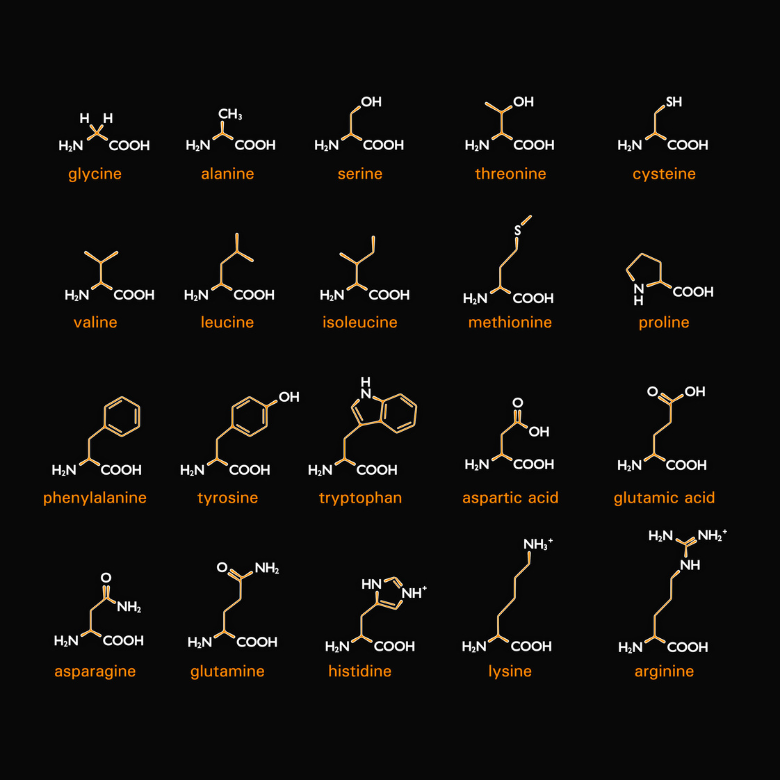
Amino asitlerin fiziko-kimyasal özellikleri
Amino asitlerin fiziksel formu genellikle tatlı bir tada sahip kristalimsi bir katıdır. Sudaki çözünürlükleri iyidir ancak organik solventlerde çözünmezler. Erime noktaları nispeten yüksektir. Amino asitlerin kimyasal yapısı amfoteriktir ve sulu çözeltilerinin reaksiyonu nötrdür. Ayrışma, temel amin grubunun bir karboksil radikaliyle nötrleştirilmesinin sonucu olan ikili iyonlar üretir. Bu, her iki yükü de gösteren bir iç amonyum tuzunun üretilmesiyle sonuçlanır: pozitif ve negatif. Miktarları eşittir. Bir amino asit ayrıştığı ortama bağlı olarak katyon veya anyon halinde bulunabilir. Asidik reaksiyonlarda karboksil grubu ayrışmaz ve amino asit pozitif yüke sahiptir. Alkali bir ortamda reaksiyonlar negatif iyon üretmeye doğru kayar.
İzoelektrik nokta (pI)
Bir amino asidin ikili iyon şeklini aldığı noktadır. Her molekül için, [H 3 O +] iyonlarının yeterli konsantrasyonunu ayarlayabiliriz; bu, iyonların elektrik alanında hareket etmediği bir pH anlamına gelir. Amino asitlerin amfoterik yapısı ve ikili iyon formundaki varlığı, asitlerden ve alkalilerden etkilendiğinde tuzların iyonik yapısını ima eder. İzoelektrik noktanın deneysel belirlenmesi, bilinen pH konsantrasyonlarına sahip çözeltiler ( CH3COOH ve CH3COONa ) içeren uygun test tüplerine bir amino asidin, örneğin kazeinin eklenmesiyle gerçekleştirilir. Yatağın en bol olduğu izoelektrik noktaya ulaşılır. İzoelektrik noktanın özelliği göz önüne alındığında, bunu elektroforez kullanarak bir protein karışımını ayırmak için kullanabiliriz. Bu yöntem, amino asitlerin asidik-bazik özelliklerine dayanır ve karışım, ıslatılmış kağıt üzerine yerleştirilir. Bilinen bir pH’ın kullanılmasıyla belirli amino asitlerin hangi formda bulunacağını belirleyebiliriz. Daha sonra kağıda voltaj verirsek pozitif yüklü amino asitler katoda (-), negatif yüklü amino asitler ise anoda (+) doğru hareket edecektir. Moleküldeki pozitif ve negatif yüklerle dengelenen nötr yüklü bileşikler aynı yerde kalacaktır.
Karboksil grubunun karakteristik reaksiyonları
- Esterleştirme, bir amino asit ile bir alkol arasındaki reaksiyonla üretilen esterlerin sentezlenmesinden oluşur. Böyle bir reaksiyonun ürünü amfoterik bir yapı göstermez ancak kullanılan aminin özelliklerini gösterir.
- Dekarboksilasyon, yani bir amino asidin bir baryum (II) hidroksit (Ba(OH) 2 ) çözeltisi varlığında ısıtılması anlamına gelir. Dönüşüm aminler üretir.
- Komplekslerin üretimi, amino asitlerin, renkli bileşiklerin (kompleks tuzlar) oluşumuna neden olan, başta bakır olmak üzere bir metalin katyonlarına bağlanma kabiliyeti ile ilgilidir.

Amin grubunun karakteristik reaksiyonları
- Birincil amin grubunu içeren amino asitleri ilgilendiren deaminasyon. Reaksiyon nitrik (III) asidin ( HNO2 ) etkisi altında meydana gelir ve reaktan olarak kullanılan amino asit oksitlenir ve bir hidrasit üretir. Amin grubu nitrojen formunda salınır. Hidrolitik deaminasyon, dekarboksilasyonla hidrolitik deaminasyon, indirgeme yoluyla deaminasyon ve desatürasyon deaminasyonu dahil olmak üzere çeşitli deaminasyon türleri vardır.
- Amino asitlerin keto asitlere dönüşmesine neden olan oksidasyon.
- Biyokimyasal reaksiyonlar – Schiff bazları olarak sınıflandırılabilecek tüm amino asitler, geçirgenlik ve dekarboksilasyon gibi biyokimyasal dönüşümler gerçekleştirebilir.
Amino asitlerin tespiti için kullanılan reaksiyonlar
- Ninhidrin reaksiyonu, reaktanların bir amino asit ve bir ninhidrin çözeltisi formunda bir reaktif olduğu renkli bir reaksiyondur. Reaksiyon karakteristik bir mor-mavi renk üretir.
- Ksantoprotein reaksiyonu, fenilalanin, tirozin veya triptofan gibi aromatik amino asitleri tespit etme yoluna bir örnektir. Konsantre nitrik (V) asit ( HNO3 ) çözeltisine maruz bırakılan bir bileşiğin rengi sarıya döner. Reaksiyon sırasında nitrik amino asit türevlerinin üretilmesinin bir sonucudur.
Amino asit kaynakları
İnsan vücudunun iyi bir fiziksel ve zihinsel durumunu sağlamak için, ona amino asitler de dahil olmak üzere her yapı malzemesinden uygun miktarlarda sağlamalıyız. Düzgün çalışması için gereken tüm amino asitlerin son derece önemli bir kaynağı tam proteinlerdir. Bunlar et, özellikle kümes hayvanları, balık, yumurta ve süt ürünlerini içerir. Süt yüksek miktarda lösin, izolösin, treonin ve triptofan içerir. Soyada lizin ve metionin bulunur. Valin pirinç, yer fıstığı, susam ve bademle birlikte, fenilalanin ise yumurta, peynir ve tahıl ürünlerine beslenmemizde yer verilerek sağlanabilir. Gıda ürünlerinde amino asitlerin varlığı yaygındır ancak beslenmemizin dengeli olması için kullandığımız ürünlerin çeşitlendirilmesi gerekir. Bunun nedeni, uygun hayati fonksiyonları sürdürmek için gerekli olan gruptan yalnızca belirli amino asitleri içermeleridir.
